1. ĐẠI CƯƠNG
Tuyến tiền liệt là tuyến sản sinh ra tinh dịch giúp nuôi dưỡng và vận chuyển tinh trùng. Ung thư tuyến tiền liệt rất phổ biến ở nam giới, đặc biệt ở Hoa Kỳ và các nước châu Âu.
Tại nước ta, khi điều kiện kinh tế ngày càng phát triển, tuổi thọ ngày càng kéo dài, ung thư tuyến tiền liệt đang dần tăng lên trong những năm vừa qua.
Về giải phẫu bệnh: hơn 90% ung thư tuyến tiền liệt là ung thư biểu mô tuyến, chủ yếu là loại biệt hóa tốt.
Giai đoạn sớm bệnh thường không có triệu chứng hoặc nhầm lẫn với u phì đại lành tính tuyến tiền liệt. Do vậy, bệnh thường phát hiện muộn, một nửa số bệnh nhân khi chẩn đoán đã có di căn xa và hay gặp di căn vào xương, phổi.
Điều trị dựa vào phân loại các yết tố nguy cơ (giai đoạn bệnh TNM, điểm Gleason, nồng độ PSA và thời gian mong đợi sống). Các phương pháp điều trị bao gồm: phẫu thuật, xạ trị (xạ trị chiếu ngoài, xạ trị áp sát), nội tiết và hóa trị.
Cấy hạt phóng xạ là phương pháp xạ trị áp sát suất liều thấp để điều trị bệnh ung thư tuyến tiền liệt. Các hạt phóng xạ được cấy trực tiếp vào tuyến tiền liệt, vì vậy khối u tuyến tiền liệt sẽ nhận được liều bức xạ cao nhất và giảm thiểu tối đa liều bức xạ đến các cơ quan xung quanh. Điều này giúp cho việc kiểm soát khối u tối ưu đồng thời bảo tồn tốt nhất các chức năng của cơ quan xung quanh, cải thiện chất lượng cuộc sống.
Cấy hạt phóng xạ điều trị ung thư tuyến tiền liệt là một trong những phương pháp điều trị cơ bản được minh chứng mang lại hiệu quả rất cao đồng thời gần như bảo tồn được các chức năng của các cơ quan lân cận như bàng quang, trực tràng, sinh dục và đã được triển khai thường quy tại các nước phát triển như Mỹ, châu Âu, tuy nhiên phương pháp này mới được triển khai ở nước ta.
2. CHẨN ĐOÁN
2.1. Chẩn đoán xác định
2.1.1. Lâm sàng
Giai đoạn sớm thường không có triệu chứng gì, có thể phát hiện bệnh qua sàng lọc cho những đối tượng có nguy cơ cao. Khi bệnh xuất hiện các triệu chứng rầm rộ như bí tiểu, tiểu máu, bệnh thường đã ở giai đoạn muộn.
Triệu chứng toàn thân: sụt cân, chán ăn, thiếu máu.
Triệu chứng tiết niệu-sinh dục: đái rắt, đái khó, bí đái, đái ngắt quãng, đái máu… Có khi đau khi xuất tinh.
Các triệu chứng di căn: đau xương, gãy xương bệnh lý, đau ngực, khó thở…
Thăm khám trực tràng: có thể thấy tiền liệt tuyến to, dính, hạn chế di động khi u đã xâm lấn ra ngoài.
2.1.2. Cận lâm sàng
- Chẩn đoán hình ảnh:
+ Siêu âm ổ bụng: đánh giá sơ bộ tình trạng khối u, phát hiện các hạch di căn, tổn thương di căn các cơ quan trong ổ bụng.
+ Siêu âm nội soi trực tràng: phát hiện tình trạng xâm lấn của u vào các tạng lân cận trực tràng, bàng quang.
+ Chụp CT scan, cộng hưởng từ: phát hiện u, mức xâm lấn và tổn thương di căn hạch.
- Y học hạt nhân:
+ Chụp xạ hình xương với 99mTc-MDP: phát hiện những tổn thương di căn vào xương. Các tổn thương xương thường gặp ở xương cột sống, xương sườn, xương cánh chậu, xương sọ…
+ Chụp PET/CTvới 18F-FDG: ít có giá trị phát hiện u nguyên phát vì u tuyến tiền liệt thường phát triển chậm nên hấp thu18F-FDG kém, nhưng giúp phát hiện chính xác di căn, tái phát, đánh giá hiệu quả các phương pháp điều trị. Có thể chụp PET/CT với 11C-Acetate cho hình ảnh u nguyên phát rõ nét hơn.
- Sinh thiết u qua tầng sinh môn hoặc qua thành trực tràng dưới hướng dẫn của siêu âm để chẩn đoán mô bệnh học.
- Chất chỉ điểm ung thư: PSA (Prostaste Specific Antigene): có giá trị sàng lọc, chẩn đoán, đánh giá kết quả điều trị, theo dõi tái phát và di căn. PSA toàn phần, liên hợp thường tăng.
Nhằm mục đích tăng độ nhạy và độ chuyên biệt của xét nghiệm PSA, các xét nghiệm chuyên sâu như đo vận tốc PSA, tỷ trọng PSA, tỷ lệ PSA tự do, PSA theo tuổi (tỷ lệ người mắc ung thư tuyến tiền liệt tăng theo tuổi, giữa hai nhóm dưới 50 tuổi và trên 50 tuổi có sự tăng vọt), ngoài ra xác định thêm tỷ lệ PSA tự do trên PSA toàn phần nếu dưới 20% thì nghi ngờ ung thư nhiều hơn.
- Xét nghiệm sinh học phân tử: Giải trình tự nhiều gen.
- Xét nghiệm máu: Calci máu, phosphatase kiềm tăng trong trường hợp có di căn xương.
2.2. Chẩn đoán phân biệt
Cần phân biệt với: viêm tuyến tiền liệt, lao tuyến tiền liệt, phì đại tuyến tiền liệt.
2.3. Chẩn đoán giai đoạn TNM theo AJCC lần thứ 8 năm 2017
T U nguyên phát
Tx Không đánh giá được u nguyên phát
T0 Không có bằng chứng của u nguyên phát
T1 U nguyên phát không có biểu hiện lâm sàng và không sờ thấy
T1a U xác định bằng mô bệnh học ở ≤5% trong tổ chức lấy được
T1b Uxác định bằng mô bệnh học ở >5% trong tổ chức lấy được
T1c U xác định bằng sinh thiết kim ở một hoặc cả 2 thùy
T2 U sờ thấy và còn khu trú trong tuyến tiền liệt
T2a U chiếm không quá 1/2 của một thùy
T2b U chiếm hơn 1/2 của một thùy nhưng vẫn ở trong 1 thùy
T2c U có cả ở 2 thùy
T3 U xâm lấn qua bao tuyến tiền liệt
T3a U xâm lấn vỏ bao một hoặc hai bên
T3b U xâm lấn túi tinh
T4 U dính hoặc xâm lấn cơ quan lân cận ngoài túi tinh: cơ thắt ngoài, bàng quang, trực tràng, cơ nâng hậu môn, thành chậu.
N Hạch vùng
Nx Không đánh giá được hạch vùng.
N0 Chưa có di căn hạch vùng.
N1 Di căn hạch vùng.
M Di căn xa
M0 Chưa di căn xa
M1 Có di căn xa
M1a Di căn hạch ngoài vùng
M1b Di căn xương
M1c Di căn cơ quan khác có hoặc không có di căn xương.
3. PHÂN LOẠI NGUY CƠ
3.1. Nguy cơ rất thấp
T1a
Điểm Gleason: ≤6
PSA <10ng/ml
PSA tỷ trọng <0,15ng/ml/g
Sinh thiết tuyến tiền liệt: <3 điểm (+), <50% tế bào (+) trong mỗi điểm.
3.2. Nguy cơ thấp
T1, T2a
Điểm Gleason: 2-6
PSA <10ng/ml.
3.3. Nguy cơ trung bình
T2b, T2c hoặc
Điểm Gleason =7 hoặc
PSA=10-20ng/ml.
3.4. Nguy cơ cao
T3a hoặc
Điểm Gleason =8-10 hoặc
PSA >20 ng/ml.
3.5. Nguy cơ rất cao
T3b, T4
N1
4. ĐIỀU TRỊ
4.1. Nguyên tắc chung
Tùy theo bảng phân loại nguy cơ lựa chọn và phối hợp những phương pháp điều trị thích hợp.
Giai đoạn khu trú: phương pháp điều trị được lựa chọn là phẫu thuật hoặc xạ trị kết hợp nội tiết.
Giai đoạn muộn: điều trị nội tiết, điều trị hóa chất khi nội tiết thất bại, xạ trị triệu chứng
4.2. Điều trị ung thư tuyến tiền liệt bằng phương pháp cấy hạt phóng xạ 125I
Là phương pháp đưa các hạt phóng xạ trực tiếp vào tuyến tiền liệt theo một kế hoạch đã được lập trước bằng một phần mềm chuyên dụng đảm bảo khối u sẽ nhận được liều bức xạ cao nhất và giảm thiểu tối đa liều bức xạ tới các cơ quan lành xung quanh. Đây là phương pháp cấy hạt phóng xạ vĩnh viễn (Permanent brachytherapy hoặc Low dose rate brachytherapy): các hạt phóng xạ (Iodine-125 hoặc Palladium-103) được cấy vĩnh viễn trong tuyến tiền liệt, liều bức xạ được giải phóng chậm trong một vài tháng.
Việc điều trị ung thư tuyến tiền liệt bằng phương pháp cấy hạt phóng xạ cần được thực hiện ở các cơ sở Y học hạt nhân có đủ điều kiện và được phép xử lý, lưu trữ và sử dụng các nguồn phóng xạ cho quy trình điều trị, theo luật an toàn bức xạ.
4.2.1. Chỉ định
- Nguy cơ thấp: cấy hạt phóng xạ điều trị áp sát đơn thuần.
- Nguy cơ trung bình: cấy hạt phóng xạ điều trị áp sát + xạ trị chiếu ngoài (40-50Gy) ± nội tiết (4-6 tháng).
Liều xạ trị:
- Cấy hạt phóng xạ với 125I liều 145Gy, với 103Pd liều 125Gy.
- Cấy hạt phóng xạ sau khi xạ trị chiếu ngoài 40-50Gy: với 125I liều 110Gy và
103Pd liều 100Gy.
4.2.2. Chống chỉ định
- Ung thư tuyến tiền liệt tổn thương rộng, di căn, thể trạng kém
- Tắc nghẽn đường bài niệu nặng
- Chống chỉ định của gây mê
- Bệnh nhân ung thư kèm bệnh lý suy tim, suy hô hấp nặng, thời gian sống thêm dưới 5 năm.
- Cần cân nhắc khi kích thước tuyến tiền liệt lớn, kích thước thùy giữa tuyến tiền liệt lớn do khả năng cấy không đạt tối ưu. Có thể điều trị liệu pháp nội tiết trước sau đó đánh giá lại xét cấy hạt phóng xạ.
4.2.3. Các bước chuẩn bị
a) Nhân lực
- Bác sĩ chuyên khoa
+ Y học hạt nhân
+ Ung bướu (có chứng chỉ xạ trị ung thư và đã được đào tạo về xạ trị áp sát và cấy hạt phóng xạ điều trị ung thư tuyến tiền liệt: tối thiểu lập kế hoạch được 5 bệnh nhân (BN), quan sát 5 BN, thực hành điều trị dưới hướng dẫn 10 BN, theo dõi 10 BN).
+ Chẩn đoán hình ảnh
+ Thận tiết niệu
+ Gây mê
- Điều dưỡng chuyên khoa
- Kỹ thuật viên chuyên khoa: gây mê hồi sức, xạ trị ung thư, y học hạt nhân
- Kỹ sư vật lý y khoa có chứng chỉ an toàn bức xạ.
b) Phương tiện
+ Hệ thống cấy hạt phóng xạ chuyên dụng
- Máy siêu âm với đầu dò chuyên dụng, độ phân giải từ (5-12MHz)
- Hệ thống giá đỡ (tấm áp)
- Hạt phóng xạ: I-125
- Kim cấy phóng xạ
- Hệ thống tải nạp hạt
- Hệ thống lập kế hoạch chuyên dụng (phần mềm lập kế hoạch xạ trị)
- Máy đo rà phóng xạ
- Thiết bị chuẩn hoạt độ phóng xạ

+ Phòng mổ
- Thuốc gây tê, gây mê, giảm đau, kháng sinh, corticoid …
- Hệ thống monitor trong khi thực hiện thủ thuật
- Máy nội soi bàng quang ống mềm
+ Phòng hồi tỉnh (chăm sóc bệnh nhân sau thủ thuật)
- Giường
- Thuốc cần thiết: kháng sinh, giảm đau, kháng viêm,…
+ Người bệnh
- Bệnh nhân được chẩn đoán xác định ung thư tuyến tiền liệt bằng mô bệnh học, có chỉ định điều trị bằng cấy hạt phóng xạ.
- Bệnh nhân và gia đình đồng ý chấp nhận kỹ thuật này.
4.2.4. Các bước tiến hành
a) Kiểm tra lại dữ liệu bệnh nhân
b) Lập kế hoạch xạ trị
- Siêu âm xác định vị trí, ranh giới, hình dạng, thể tích u.
- Xác định liều xạ, lập kế hoạch xạ trị.
Liều xạ đối với thể tích lập kế hoạch PTV: 108-110Gy
Mục tiêu kế hoạch xạ trị:
Thể tích đích lâm sàng (Clinical Target Volume, CTV):
- V100CTV (tỷ lệ phần trăm thể tích CTV nhận được 100% liều điều trị) ≥95%
- V150CTV (tỷ lệ phần trăm thể tích CTV nhận được 150% liều điều trị) ≤50%
- D90CTV (liều bao phủ trên 90% thể tích CTV) > liều chỉ định
Trực tràng:
- D2ccrectum (liều tối thiểu trong 2mm3 thể tích trực tràng bị chiếu xạ) < liều chỉ định
- D0.1ccrectum (liều tối thiểu trong 0,1mm3 thể tích trực tràng bị chiếu xạ) <200Gy
Niệu đạo:
- D10%urethra (liều tối thiểu trong 10% niệu đạo đoạn tiền liệt) <150% liều chỉ định
- D30%urethra (liều tối thiểu trong 10% niệu đạo đoạn tiền liệt) <130% liều chỉ định
- Bác sĩ Y học hạt nhân kiểm tra lại số lượng hạt cần dùng và khoảng cách giữa các hạt.
- Chuẩn bị kim cấy hạt phóng xạ theo kế hoạch

c) Tiến hành cấy hạt phóng xạ
- Tiến hành cấy hạt phóng xạ theo kế hoạch dưới hướng dẫn của siêu âm.
- Siêu âm xác định lại phân bố các hạt phóng xạ trong u.
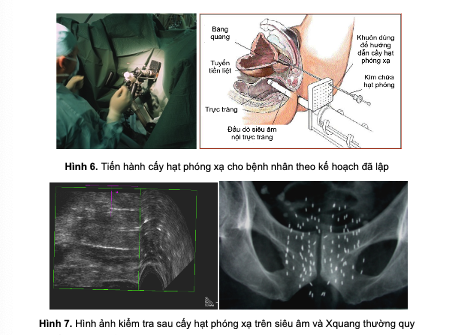
+ Kiểm tra sau cấy hạt phóng xạ
- Chụp Xquang tiểu khung đánh giá sự phân bố các hạt phóng xạ (Hình7).
- Nội soi bàng quang kiểm tra bảo đảm không có tổn thương bàng quang, đo hoạt độ phóng xạ trong nước tiểu.
4.2.5. Các biến chứng
- Tác dụng phụ trong quá trình cấy hạt phóng xạ: có thể gây tổn thương các cơ quan xung quanh như bàng quang, trực tràng, đại tràng, ruột non… tuy nhiên có thể phát hiện và xử lý kịp thời do có sự hướng dẫn của siêu âm trong quá trình điều trị.
- Tác dụng phụ sau cấy hạt phóng xạ:
+ Triệu chứng về tiết niệu-sinh dục:
Thường gặp là tiểu nhiều lần, tiểu dắt, tiểu buốt, các triệu chứng này sẽ hết sau 4-6 tuần.
Bí tiểu, tiểu không tự chủ
Tiểu máu: thường hết sau 3-5 ngày
Rối loạn chức năng dinh dục: ít gặp
+ Triệu chứng về tiêu hóa:
Đau rát, chảy máu trực tràng
Rối loạn tiêu hóa (ỉa chảy), đại tiện không tự chủ
+ Một số tác dụng phụ khác: mệt mỏi, cảm giác khó chịu ở vùng chậu, viêm nhiễm vùng da giữa bìu và hậu môn…
- Tác dụng phụ muộn:
+ Viêm trực tràng mạn tính
+ Viêm bàng quang mạn tính
+ Tiểu khó do hẹp niệu đạo
+ Rối loạn cương dương, liệt dương: ít gặp
5. PHÒNG BỆNH
Cần khám lâm sàng (thăm trực tràng), siêu âm tuyến tiền liệt và định lượng PSA định kỳ ở những người đàn ông trên 50 tuổi. Tiến hành sinh thiết xét nghiệm mô bệnh học khi u tuyến tiền liệt rắn, nồng độ PSA >4ng/ml.
TÀI LIỆU THAM KHẢO
1. Nguyễn Bá Đức (2010). Hướng dẫn thực hành chẩn đoán bệnh ung thư, chẩn đoán và điều trị ung thư tiền liệt tuyến. Nhà xuất bản Y học.
2. Mai Trọng Khoa (2015). Hướng dẫn chẩn đoán và điều trị bệnh bằng Y học hạt nhân. Nhà xuất bản Y học
3. Mai Trọng Khoa (2014). Hướng dẫn chẩn đoán và điều trị một số bệnh ung bướu. Nhà xuất bản Y học.
4. Trần Văn Thuấn, Lê Văn Quảng, Nguyễn Tiến Quang (2019). Hướng dẫn chẩn đoán điều trị bệnh ung thư thường gặp. Nhà xuất bản Y học
5. Mai Trọng Khoa (2016). Kháng thể đơn dòng và phân tử nhỏ trong điều trị bệnh ung thư. Nhà xuất bản Y học.
6. Mai Trọng Khoa (2013). Ứng dụng kỹ thuật PET/CT trong ung thư. Nhà xuất bản Y học.
7. Bộ môn Ung thư Trường Đại học Y Hà Nội (2011). Bài giảng ung thư học, ung thư tiền liệt tuyến. Nhà xuất bản Y học, tr: 224-227.
8. Mai Trọng Khoa (2012). Atlas PET/CT một số bệnh ung thư ở người Việt Nam. Nhà xuất bản Y học.
9. Mai Trọng Khoa và cộng sự (2012). Y học hạt nhân (Sách dùng cho sau đại học). Nhà xuất bản Y học.
10. Hội Tiết niệu - Thận học Việt Nam (2018). Phác đồ hướng dẫn chẩn đoán và điều trị ung thư tuyến tiền liệt.
11. American Society for Radiation Oncology (ASTRO) and American College of Radiology (ACR) (2018). Practice Guideline for transperineal permanent brachytherapy of prostate cancer.
12. Brian J Davis, Eric M Horwitz, W. Robert Lee, et al (2012). American Brachytherapy Society consensus guidelines for transrectal ultrasound guided permanent prostate brachytherapy. Brachytherapy 11 (2012) 6-19.
13. Peter D. Grimm D.O., John E. Sylvester M.D., et al (2009). “Low and Intermediate Risk Prostate Cancer - Comparative Effectiveness of Brachytherapy, Cryotherapy, External Beam Radio Therapy, HIFU, Proton Therapy, Radical Prostatectomy and Robot Assisted Radical Prostatectomy”, accepted for publication and presentation at the 51st American Society for Radiation Oncology Annual Meeting, abstract, Chicago, IL, November 1-5, 2009.
14. Vicent T DeVita, Theodore S. Lawrence, Steven A. Rosenberg (2008). Prostate cancer. Principles and Practice of Oncology, 7th edition. Lippincott Williams and Wilkins. pp 431-434.
15. The Royal College of Radiologists (2012). Quality assurance practice guidelines for transperineal LDR permanent seed brachytherapy of prostate cancer. London.
16. National Comprehensive Cancer Network (2019). Prostate cancer, version 2.2019. NCCN Clinical Practice Guideline in Oncology.
17. Janet F. Eary, Winfried Brenner (2007). Nuclear medicine therapy. Informa Healthcare USA, Inc. 270 Madison Avenue New York
18. Christiaan Schiepers (2006). Diagnostic Nuclear Medicine, 2nd Revised Edition. Springer - 2. Verlag Berlin Heidelberg.
19. Ell P.J., S.S. Gambir (2004). Nuclear Medicine in Clinical Diagnosis and Treatment. Churchill Livingstone.
20. Hans. Jỹrgen Biersack, Leonard. M. Freeman (2007). Clinical Nuclear Medicine. Springer-7. Verlag Berlin Heidelberg.
21. Hagop M. Kantarjian, Robert A. Wolff, Charles A. Koller (2006). The MD Anderson manual of medical oncology. McGraw-Hill.
22. Janet FE, Winfried B (2007). Nuclear medicine therapy. Informa heathcare. New York. London.
- Đăng nhập để gửi ý kiến

